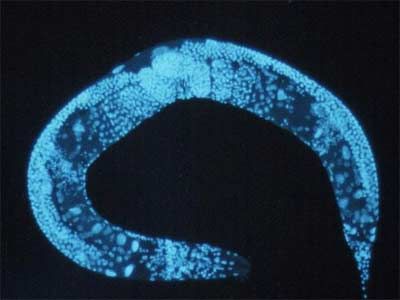
C. elegans, un nématode qui possède des gènes de réparation de l'ADN communs avec ceux de l'humain.
Cette méthode, pour laquelle il vient d’obtenir un brevet américain, pourrait augmenter l’efficacité des traitements de radiothérapie ou de chimiothérapie si on parvenait à l’appliquer aux cellules cancéreuses. «L’idée est d’interférer avec le mécanisme naturel de réparation de l’ADN de façon à ce que les bris induits dans le matériel génétique par les traitements entraînent plus facilement la mort des cellules cancéreuses», résume-t-il. En conditions normales, certaines activités essentielles au fonctionnement de la cellule sont suspendues le temps que l’ADN soit réparé. L’entrée en scène d’une enzyme qui joue un rôle clé dans le processus de réparation cellulaire, la PARG, permet la reprise de ces activités. Serge Desnoyers a eu l’idée de recourir à de petits ARN interférents pour entraver l’activité de la PARG, plaçant ainsi la cellule dans un état permanent de réparation, incompatible avec son fonctionnement normal. Si son raisonnement tenait la route, les petits ARN interférents devaient stopper la division cellulaire et provoquer une mortalité accrue des cellules soumises à un rayonnement nocif.
Les tests qu’il a menés à l’aide de C. elegans, un nématode qui possède des gènes de réparation de l’ADN communs avec ceux de l’humain, ont confirmé ses deux prédictions. En présence de petits ARN interférents, les oeufs de C. elegans cessent leur développement et le taux de mortalité des spécimens adultes exposés à un même rayonnement passe de 29 % à 80 %, rapporte le chercheur dans sa demande de brevet. «Nous allons maintenant tenter de démontrer que ce que nous avons observé chez C. elegans s’applique aux cellules cancéreuses des mammifères. Il me semblait toutefois important d’obtenir un brevet pour cette méthode dès maintenant parce que l’idée circulait depuis un certain temps parmi les chercheurs actifs dans mon domaine», précise-t-il.
Le professeur Desnoyers reconnaît qu’il reste encore des obstacles importants à franchir avant que cette méthode ne soit utilisée dans le traitement des personnes atteintes de cancer, notamment le mode de livraison des petits ARN interférents dans les cellules cancéreuses. «Nous espérons que la recherche dans ce domaine aura progressé lorsque nous serons rendus à faire des essais chez l’humain dans quelques années», ajoute-t-il.