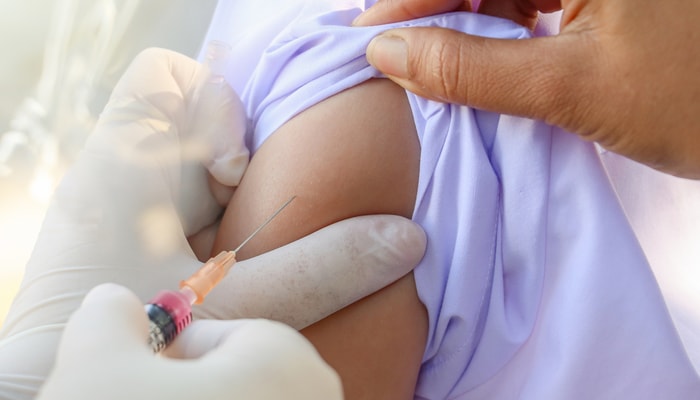
La valve cardiaque après la dissolution du moule en sucre et avant la mise en culture dans le bioréacteur. Le milieu de culture cellulaire, le liquide rouge, contient des nutriments pour les cellules.
— Courtoisie
Du sucre, du gel à base d'algues et des cellules humaines, voilà les trois ingrédients nécessaires pour fabriquer des valves cardiaques artificielles. Jean Ruel, professeur au Département de génie mécanique et de génie industriel, développe cette recette depuis 10 ans.
«C'est un organe qui est difficile à reproduire», lance le chercheur, membre du Centre de recherche en organogénèse expérimentale de l'Université Laval (LOEX) et du Centre de recherche du CHU de Québec – Université Laval.
Actuellement, deux types de valve de remplacement sont utilisés en clinique. Les valves mécaniques sont fabriquées en matériaux inertes, alors que les bioprothèses sont faites à base de tissu animal. Ces approches ont toutefois leurs inconvénients, souligne le professeur Ruel. Les valves mécaniques nécessitent la prise d'anticoagulants et la durée de vie des bioprothèses est limitée, car elles se dégradent avec le temps. Ces deux valves sont aussi inadaptées pour les jeunes. «Les enfants qui naissent avec un problème de valve cardiaque doivent subir plusieurs opérations dans leur vie parce que leur corps et leur cœur grandissent», ajoute le chercheur.
Une nouvelle approche de fabrication
Pour pallier ces enjeux, Jean Ruel et son équipe ont travaillé sur un procédé de fabrication novateur basé sur l'impression 3D. D'abord, un moule de la valve est imprimé avec du verre en sucre, semblable aux sculptures comestibles utilisées en pâtisserie. De l'hydrogel, une sorte de gel semi-solide à base d'eau et d'algues, est mélangé avec des cellules humaines en suspension puis versé dans le moule. «Les cellules utilisées proviennent du tissu adipeux. On pourrait envisager un prélèvement directement chez le patient pour éliminer le problème de biocompatibilité», précise le professeur.
Une fois le mélange d'hydrogel assez solidifié, le moule de sucre est dissout. À cette étape, l'équipe dépose la valve dans un bioréacteur qui sert d'incubateur pour favoriser la reproduction des cellules humaines. «En quelques semaines, elles sont capables de former une structure plus solide en sécrétant des agents comme du collagène.»

La valve reste plusieurs jours dans le bioréacteur avant d'être entraînée dans le simulateur d’écoulement cardiaque.
— Courtoisie
Une valve qui s'adapte au corps
Une fois la structure formée, elle doit apprendre à fonctionner comme une vraie valve. Pour ce faire, elle est insérée dans un simulateur d'écoulement cardiaque pour l'entraîner à réagir au passage du sang dans le cœur. Dans ces conditions plus réalistes, les cellules vont adapter la structure de la valve pour répondre à la pression sanguine. «C'est après cette étape qu'on pourrait implanter la valve chez la personne», indique Jean Ruel.
Il ajoute qu'«avec une échographie, on est capable de voir et de mesurer la valve du patient et de reproduire sa géométrie avec l'impression 3D. Et comme les cellules contenues dans l'hydrogel peuvent s'adapter, la structure de la valve pourrait se remodeler pour répondre à la croissance du patient, comme une valve naturelle». La valve ainsi produite a l'avantage d'être biocompatible, adaptée à la géométrie du cœur et capable de grandir avec la personne.
La valve étant encore à l'étape du laboratoire, les scientifiques souhaitent maintenant en améliorer la durabilité. Des essais dans des modèles animaux pourraient ensuite être envisagés pour éventuellement atteindre une utilisation chez l'humain.
Selon le professeur Jean Ruel, ce procédé de fabrication des valves pourrait éventuellement être automatisé pour répondre à la demande, ce qui favoriserait son adoption en clinique.
Les signataires de l'étude, publiée dans la revue Biofabrication, sont Yannick Rioux, Julie Fradette, Cindy Jean Hayward, Viviane Séguin, André Bégin-Drolet et Jean Ruel, tous affiliés à l'Université Laval.