— Getty Images/Peterschreiber.media
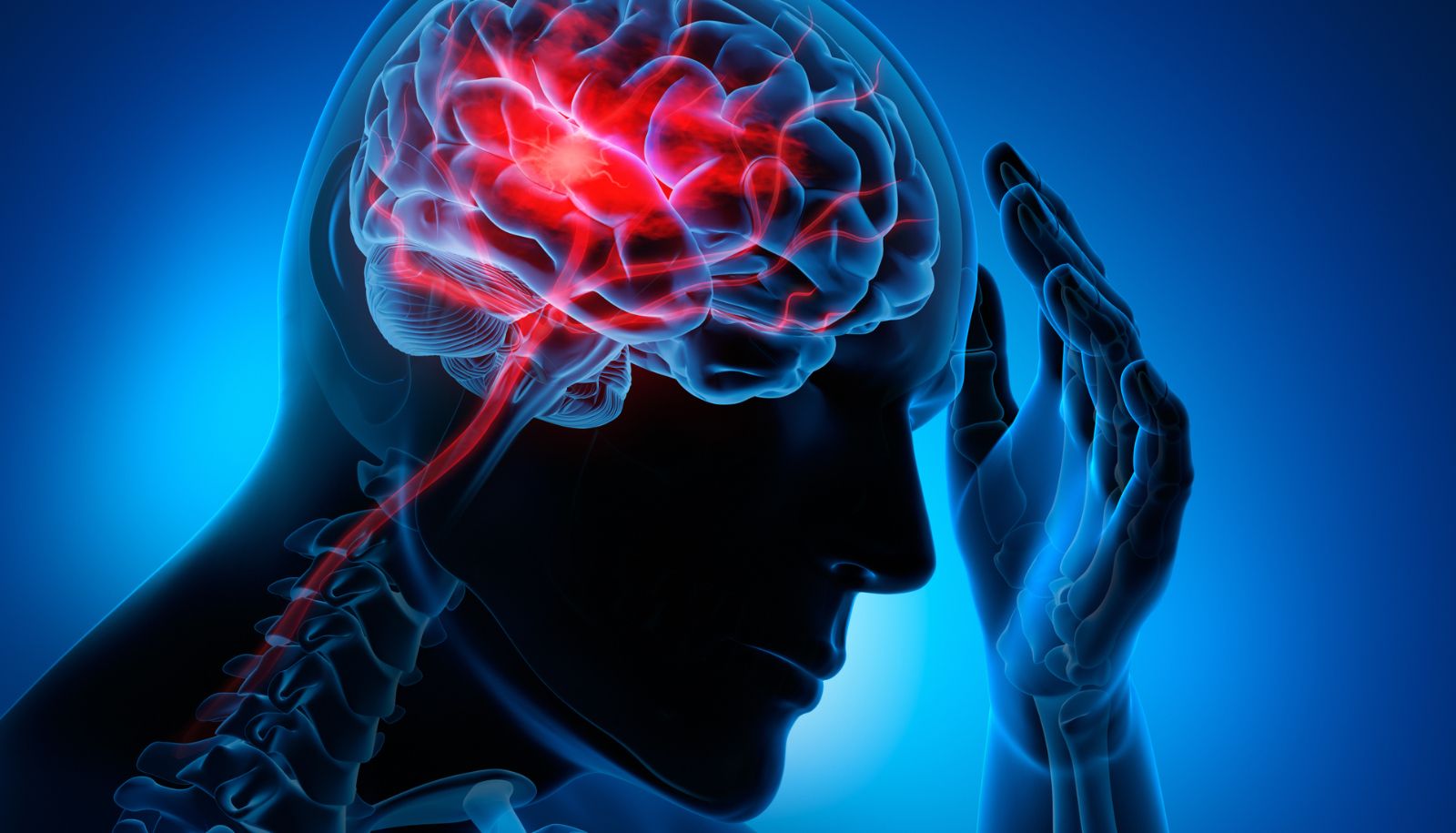
Des chercheurs de l'Université Laval ont mis en lumière le rôle clé d'une protéine du cerveau dans la réparation des tissus endommagés à la suite d'un accident vasculaire cérébral (AVC). Leur percée, qui vient de faire l'objet d'une publication dans la revue Cellular and Molecular Life Sciences, laisse entrevoir la possibilité de recourir à cette protéine pour mettre au point un nouveau traitement destiné aux personnes victimes d'AVC.
La protéine en question, la PDGF-D, a été découverte il y a une dizaine d'années. «Chez la souris, cette protéine est produite transitoirement dans le cerveau après un AVC par des cellules qui tapissent l'intérieur des vaisseaux sanguins, les cellules endothéliales. Le pic de production de cette protéine survient trois jours après l'AVC. La PDGF-D est aussi produite chez l'humain, mais sa fonction dans le cerveau n'était pas encore connue», précise le responsable de l'étude, Ayman ElAli, professeur à la Faculté de médecine de l'Université Laval et chercheur au Centre de recherche du CHU de Québec-Université Laval.
Les seuls récepteurs connus de la PDGF-D se trouvent sur des cellules, appelées péricytes, qui sont situées à l'interface entre les cellules nerveuses et les vaisseaux sanguins du cerveau. C'est ce qui a poussé les chercheurs a étudié le lien qui existait entre les péricytes et la PDGF-D. «Les péricytes sont des cellules spécialisées qui jouent un rôle essentiel dans la régulation du débit sanguin cérébral et qui servent d'interface pour les échanges entre le sang et les cellules nerveuses, précise le professeur ElAli. On sait qu'un AVC peut provoquer la mort des péricytes ou perturber leur fonctionnement.»
Afin de comprendre comment la PDGF-D affecte les péricytes, les chercheurs ont d'abord induit une sous-expression de cette protéine chez des souris utilisées comme modèle d'étude pour l'AVC. «Dans les jours qui ont suivi l'AVC, nous avons constaté que la diminution de la PDGF-D était associée à une plus forte mortalité des neurones, à une réduction de la densité des microvaisseaux et à une occlusion des nouveaux vaisseaux qui se formaient dans leur cerveau», signale le professeur ElAli.
L'expérience suivante, qui consistait à administrer la protéine PDGF-D dans la cavité nasale des souris après un AVC, a livré des résultats diamétralement opposés. «Nous avons observé une augmentation de la survie des neurones et un meilleur rétablissement neuronal. De plus, la densité des vaisseaux sanguins cérébraux a augmenté, ce qui a conduit à une amélioration du débit sanguin dans le cerveau.»
Des expériences menées in vitro avec des cellules endothéliales et des péricytes prélevés chez l'humain ont conduit à ces conclusions similaires.
«Nos résultats suggèrent que la protéine PDGF-D est un appel à l'aide que les vaisseaux sanguins lancent aux péricytes après un AVC, explique le professeur ElAli. Ce S.O.S. stimule les péricytes qui réagissent en assurant le maintien de la structure et des fonctions des vaisseaux sanguins ainsi que la production de nouveaux vaisseaux sanguins. Grâce à cela, l'oxygène et les nutriments essentiels à la survie des neurones et à la réparation des tissus endommagés par l'AVC peuvent être acheminés dans le cerveau.»
— Ayman ElALi
À la lumière de ces résultats, l'idée d'administrer la protéine PDGF-D à des personnes qui viennent de subir un AVC s'impose spontanément à l'esprit. «C'est une molécule qui existe naturellement dans le corps, nous savons comment la synthétiser en laboratoire et il est possible de l'administrer de façon non invasive par voie nasale. Techniquement, son utilisation pour atténuer les dommages causés par un AVC et pour favoriser la réparation des tissus est envisageable. Il reste à en faire la démonstration chez l'humain», conclut le professeur ElAli.
Les autres auteurs de l'étude parue dans Cellular and Molecular Life Sciences sont Maxime Bernard, Romain Menet et Sarah Lecordier.