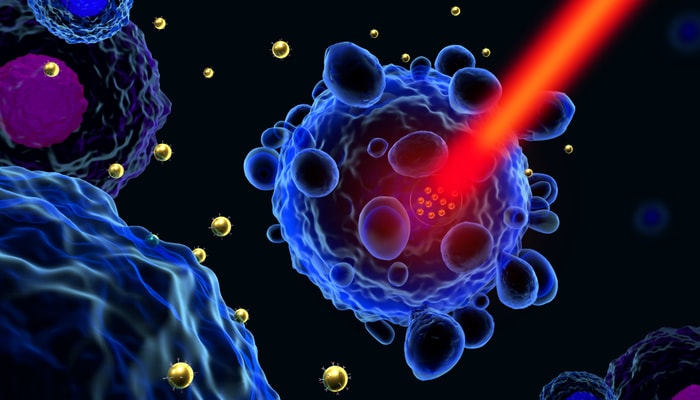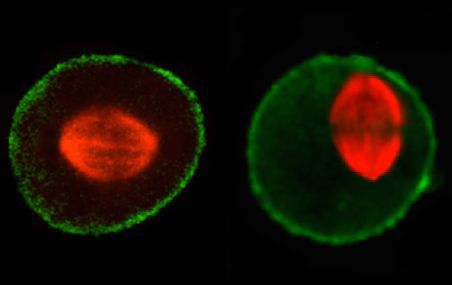
À gauche, le fuseau de microtubules (en rouge), sur lequel se déplacent les chromosomes, se positionne au centre de la cellule au moment de la division cellulaire. À droite, dans une cellule qui n'exprime pas les protéines chaperons BAG3 ou HSPB8, le fuseau ne parvient pas à se centrer, comme s'il était mal amarré. Ce défaut peut conduire à une mauvaise ségrégation du matériel génétique et à la mort des cellules filles issues de cette division aberrante.
Les deux protéines en question, appelées BAG3 et HSPB8, forment un complexe bien connu pour son rôle dans l'autophagie, un processus qui s'enclenche lorsqu'une cellule est soumise à un stress lui causant des dommages. Les protéines ou les organelles touchées sont démantelées par un arsenal moléculaire, qui inclut les deux protéines chaperons, et leurs composantes sont recyclées. «BAG3 et HSPB8 ont d'autres fonctions connues, ajoute la professeure Lavoie. Elles sont associées aux structures du cytosquelette qui assurent le soutien et la mobilité de la cellule et qui interviennent dans le changement de forme qui survient, entre autres, au moment de la division cellulaire. Des études ont aussi montré que BAG3 est surexprimé dans des cellules cancéreuses en multiplication rapide où elle intervient dans la dynamique du cytosquelette.»
Afin de pousser un peu plus loin les connaissances sur le complexe BAG3-HSPB8, la chercheuse et ses collaborateurs du Centre de recherche du CHU de Québec-Université Laval ont comparé la division de cellules cancéreuses exprimant les protéines chaperons à celle de cellules dans lesquelles leur expression avait été supprimée par manipulation génétique. Les images obtenues par microscopie confocale parlent d'elles-mêmes.
Dans une cellule non modifiée (vidéo MP4, 550 Ko), le fuseau de microtubules (en rouge), sur lequel se déplacent les chromosomes, se forme et se positionne au centre de la cellule. Ce fuseau est attaché au cortex d'actine (en vert) situé en périphérie de la cellule. Progressivement, le fuseau se divise en deux, chaque partie emportant la moitié des chromosomes. La membrane cytoplasmique s'invagine et, au terme d'un processus qui requiert une soixantaine de minutes, deux cellules filles sont formées.
Les choses se passent moins rondement dans les cellules sans BAG3 (vidéo MP4, 450 Ko). Le fuseau dérive dans la cellule et il ne parvient pas à se centrer, comme s'il était mal amarré. «Après quelques heures, la cellule finit par se diviser, mais la probabilité qu'il y ait une mauvaise ségrégation du matériel génétique est forte, souligne Josée N. Lavoie. Les cellules qui en résultent vont tenter de se diviser de nouveau, mais plusieurs finiront par mourir. Nous obtenons les mêmes résultats avec les cellules sans HSPB8. Notre hypothèse est qu'en absence des deux protéines chaperons, le désassemblage des complexes protéiques indispensables à la reconfiguration du cytosquelette au moment de la division cellulaire ne peut se dérouler efficacement dans les cellules en division rapide.»
Le complexe BAG3-HSPB8 constitue donc une cible potentielle pour ralentir ou stopper la prolifération de cellules cancéreuses. «En principe, ce complexe ne serait pas indispensable à la division cellulaire dans tous les types de cellules, mais il faciliterait la multiplication rapide des cellules cancéreuses», ajoute la professeure Lavoie.
L'étude parue dans PLOS Genetics est signée par Margit Fuchs, Carole Luthold, Solenn M. Guilbert, Alice Anaïs Varlet, Herman Lambert, Alexandra Jetté, Sabine Elowe, Jacques Landry et Josée N. Lavoie.