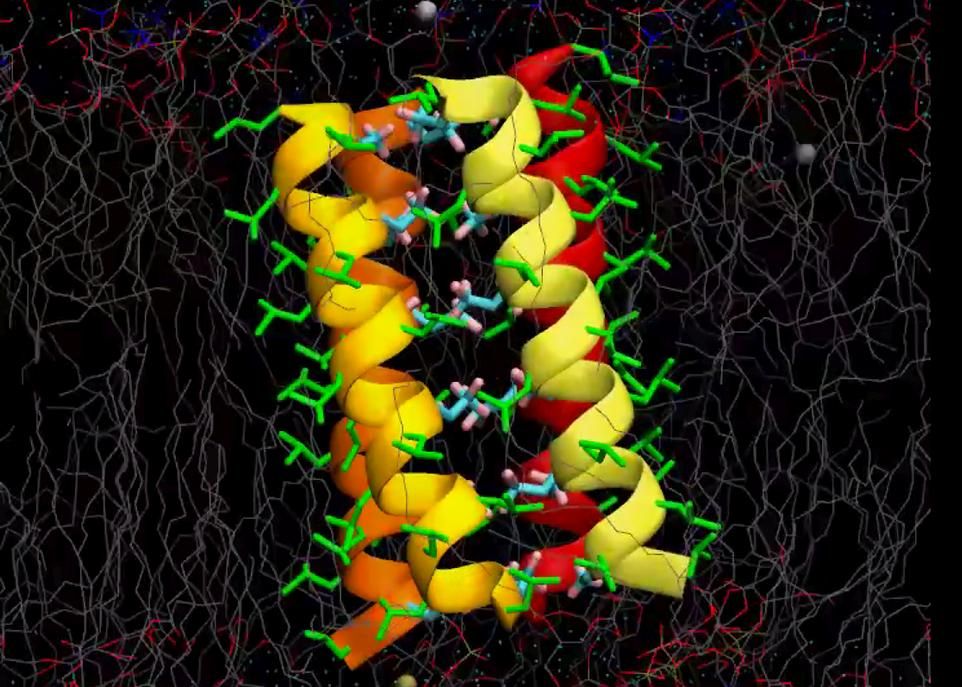
Le composé préparé par les chercheurs contient 21 acides aminés, dont 6 sont fluorés. Lorsqu'ils sont placés dans une membrane cellulaire, ces composés s'assemblent par groupe de quatre, formant quatre hélices au centre desquelles les ions peuvent circuler.
— Laboratoire de Normand Voyer
Plusieurs équipes de chercheurs étaient déjà parvenues à fabriquer des canaux ioniques artificiels, mais leur instabilité limitait les usages qu'on pouvait en faire. «Nous avons tiré profit de certaines caractéristiques des atomes de fluor pour corriger ce problème, souligne le professeur Voyer. Les canaux que nous avons produits ont une stabilité telle qu'on pourrait les utiliser dans plusieurs applications médicales sur le plan tant diagnostique que thérapeutique.»
Pour produire ces canaux, les chercheurs ont préparé un composé contenant 21 acides aminés, dont 6 sont fluorés. Lorsqu'ils sont placés dans une membrane cellulaire, ces composés s'assemblent par groupe de quatre, formant quatre hélices au centre desquelles les ions peuvent circuler (voir l'animation). Cet assemblage a une longueur de 3,2 nanomètres, ce qui est suffisant pour traverser une membrane cellulaire, et il affiche une sélectivité pour le sodium. «Les atomes de fluor sont orientés vers l'intérieur du canal et ils agissent comme des sites relais pour faciliter le passage des ions sodium, signale Normand Voyer. L'extérieur du canal est hydrophobe, ce qui lui permet d'entrer à l'intérieur de la membrane des cellules.»
Les chercheurs ont démontré que ces nanostructures fonctionnaient dans des cellules artificielles. La prochaine étape consiste à les intégrer dans des ovocytes de grenouille et, à moyen terme, dans des cellules de mammifère. À partir de là, de nombreuses applications peuvent être envisagées en greffant des molécules-appâts à ces canaux. «On peut penser, par exemple, à associer ces canaux à des molécules pour lesquelles certains virus ont une affinité particulière, avance le professeur Voyer. Il suffirait qu'une seule particule virale vienne se fixer à cette molécule et qu'elle obstrue l'entrée du canal ionique pour qu'elle en modifie la conductivité. Un tel changement permettrait de confirmer la présence d'un virus chez un patient. On pourrait aussi recourir à la même stratégie pour reconnaître des cellules cancéreuses et y intégrer des canaux ioniques artificiels qui déstabiliseraient leur équilibre ionique afin de les détruire.»
L'étude de Plos One est signée par Raphaël Godbout, Maud Auger, Claudia Carpentier, François Otis, Michèle Auger et Normand Voyer, du Département de chimie, et par Sébastien Légaré et Patrick Lagüe, du Département de biochimie, de microbiologie et de bio-informatique.